Vyvchennya elektroprovidnosti vandens razmeny geriamosios sodos. Romos daktaro valandomis pasakysiu pedantui apie sodi saugojimą, niekas nesupras Vandens kaip elektros laidininko
Doslednitska robotas „Vivchennya geriamosios sodos vandens paskirstymo elektrinis laidumas“
Įėjimas
Soda buvo žinoma žmonėms maždaug du ar du tūkstančius metų prieš mūsų laiką, o gal ir anksčiau. Її buvo matomi iš sodos ežerų ir buvo matomi iš daugelio genčių šalia mineralų. Pirmieji pranešimai apie sodos pašalinimą sodos ežerų vandens virinimo būdu žinomi iki 64-ųjų mūsų gyvenimo metų. Iki XVIII amžiaus visų kraštų alchemikai atrodė tarsi kalba, tarsi šnypštė iš tokių dujų matymo, kai jiems tą rūgščių – octovoy ir sirchanoy – valandą buvo pučiama. Romėnų gydytojo Dioskorido Pedanijaus valandomis apie sodos saugojimą nieko nebuvo kalbama. 1736 m. prancūzų chemikui, gydytojui ir botanikui Henri Louie Duhamel de Monceau pirmą kartą pavyko išgauti net gryną sodą iš sodos ežerų vandens. Jūs galėjote jį sumontuoti per atstumą, kad soda atkeršytų cheminiam elementui „Natr“. Rusijoje Petro Didžiojo laikais soda buvo vadinama „zoda“ arba „sverbіnyam“, o iki 1860 m. її buvo importuojama iš už kordono. 1864 m. Rusijoje pasirodė pirmasis sodos gamykla, naudojant prancūzo Leblanc technologiją. Pačioje savo gamyklų atsiradimo pradžioje soda tapo prieinama ir atvėrė savo galimybes kaip cheminė, kulinarinė ir navitinė likarsky zasib.
У промисловості, торгівлі та в побуті під назвою сода зустрічаються кілька продуктів: кальцинована сода - безводний вуглекислий натрій Na2СO3, двовуглекисла сода - бікарбонат натрію NaНСO3, часто звана також питною содою, кристалічна сода Na2СO3 10Н2O і Nа2СO3 Н2 Сучасна харчова сода - типовий промисловий продукт
Pasaulio šviesoje įvairios Viktorijos upėje virpinamas milijonų tonų sodos pabarstymas.
Soda yra bagatolika kalba, її zastosuvannya kitaip. Soda vikoristovuyut iš Kharchovoy pramonės į metalurgiją. Zatsіkavivsya tsієyu rechovina, jakas є prie odos kabinoje ir virіshiv vivchiti, jakai rodo skirtingą sodos vandens varianto dominavimą pūdymuose, temperatūros ir koncentracijos skirtumai.
Otzhe, prieš mus buvo meta:
Dolіdit zalezhnіt elektroprovіdnіnostі vodnoe razvitie soda soda vіd vіd temperatūra і concentrаії ії vodії rozov.
Vadovas:
Perskaitykite literatūrą tolesnių veiksmų tema.
Atlikite eksperimentą su žiniomis apie šviežių galų sąstingį apie grub soda.
Sužinokite, kaip paruošti įvairių koncentracijų maistinę soda.
Doslidit zalezhnist elektroprovіdnostі vіd kontsentratsії razheniy temperatūra.
Tolesnių veiksmų faktas:
Soda bagatolika kalba, її zastosuvannya kitaip. Soda vikoristovuyut iš Kharchovoy pramonės į metalurgiją. Žinokite її vlastіvostі-iš tikrųjų zavzhdi.
Skaidrėje parodytos pagrindinės sodos vartojimo sritys.
chemijos pramonė
lengvas vekselis
tekstilės industrija
Charchovos promislovistas
medicinos profesija
metalurgija
Taip pat chemijos pramonėje - barvnikų, putplasčio ir kitų organinių produktų, fluoro reagentų, butilo chemijos gaminių gamybai.
Metalurgijoje - su retųjų žemių metalų nusodinimu ir rūdų flotacija.
Tekstilės pramonėje (siūlių tobulinimas ir audinių papildymas).
Lengvas meistriškumas - podirvio dervų ir gabalinių shkirų gamyboje, shkiryan gamyboje (škirų įdegis ir neutralizavimas).
Maisto pramonėje - kepykla, konditerijos gaminių gamyba, gėrimų ruošimas.
Medicinos pramonėje - injekciniams produktams, vaistams nuo tuberkuliozės ir antibiotikų ruošimui
Išmokęs teorinę medžiagą, išmokau iš savo kurso draugų, kurie žino smirdėjimą, tam tikrame gudravime su vikoristovuetsya kharcheva soda:
Grobyje
Charchovos promislovistas
Vaistas
Chemijos pramonė
metalurgija
Lengvas pasižadėjimas
Apklausos rezultatų ašis: didžiausias apklausoje dalyvavusių respondentų skaičius:
Pobuti -63%
Charchovos promislovistas-71 proc.
Chemijos pramonė - 57%, mažiausiai respondentų nurodė, kad labiausiai paplitusi metalurgijoje ir lengvojoje pramonėje.
Tolesniems tyrimams man reikėjo paruošti įvairių koncentracijų vandeninį tirpalą.
Hipotezė
Taip pat, siekiant padidinti vandens kiekio koncentraciją mailiaus sodoje, padidės elektros laidumas.
II. eksperimentinė dalis
„Mažiaus sodos vandens paskirstymo elektrinio laidumo tyrimai“
Meta: perekonatis, scho vandens lygiu soda є nosії elektriki - іoni, yakі veda elektros srovė.
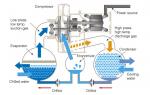
Įrengta: charčiovinė soda, chemijos kolbos iš karščiui atsparaus sandėlio, elektrodai, sprogdinimo smiginiai, gyvybės dzherelo, ampermetras, voltmetras, raktas, laboratoriniai laidai, laidai, termometras, elektrinė viryklė. 1 dokumentas
Meta: Sužinokite, kaip paruošti skirtingų koncentracijų vandeninį sodos tirpalą.
Įranga: chemikalų kolbos iš karščiui atsparaus stiklo, filtruotas vanduo, vaga, rіznovagi, Charchova soda.
Vikonanny dosvіdu:
Nuo teresos priklauso 4 g chachovoy sodos;
Į cheminę kolbą supilkite 96 ml. filtruotas vanduo;
Gurkšnokite sodą iš kolbos su vandeniu, gerai išmaišykite;
Pakartokite 8% ir 12% skirtumo paruošimo užsakymą
Nr. Sodos masė (g) Vandens kiekis (ml) Sodos koncentracija (%)
1 4 96 4
2 8 92 8
3 12 88 12
Eksperimentiniu būdu išmokau pasigaminti įvairių koncentracijų vandens rūšių pikantišką sodą.
2 sertifikatas
Paskirtis: atnešti, mokyklų mainai zbіlshennyam koncentracijos soda zbіlshuєєєї її elektroprovіdnіstі.
Įrengta: trys kolbos su įvairia skirtingos koncentracijos maistine soda, stiklainis gyvybės, ampermetras, voltmetras, spjaudymo smiginis, raktas, elektrodas.
Pithomium opir yra skaliarinė vertė, skaitinė lygi vienodo vieno ilgio ir vieno ploto cilindrinio laidininko atramai. Kuo didesnė laidininko medžiaga, tuo didesnė jogo elektrinė opir.
Gyvūnų palaikymo vienetas yra ommetras (1 omas m).
Vikonanny dosvіdu:
Schemai pasirinkite elektrinį lansyugą;
Įdėkite elektrodą į cheminę kolbą, kurioje yra 4%, 8% ir 12% sodos;
Paimkite ampermetro ir voltmetro rodmenis;
Razrahuvat opіr rozchina;
Razrahuvat elektroprovіdnіst rozhchin.
2 lentelė
Sodos koncentracija I (A) U (B) R (Ohm) λ=1 R (1Ohm=Sm)1 4 1,0 6 6 0,17
2 8 1,4 6 4,9 0,23
3 12 1,7 6 3,53 0,28
Įrodymui schemai buvo pasirinktas elektrinis strypas. Keičiant vandens skirtumo koncentraciją, registruojami ampermetro ir voltmetro rodmenys.
Vimeracija buvo atlikta 180 C temperatūroje ir 757 mm Hg atmosferos slėgyje.
Visnovok: Eksperimentiniu būdu išmokau nustatyti sodos elektrinį laidumą ir perėjau į tą, kurio koncentracija didesnė, tuo didesnis sodos elektrinis laidumas. Ir opir razchinu zі zbіlshennyam koncentracija zmenshuєtsya. Be to, esant 12% skirtumo tarp kepimo sodos, elektros laidumas bus didžiausias, o opir - mažiausias.
Dosvіd 3. "Elektrinio laidumo kritimo pagrįstumas priklausomai nuo temperatūros ir skirtumo"
Tsіl: Dar kartą apsvarstykite, kad elektros laidumas keičiasi keičiantis temperatūrai.
Komplektacijoje: trys buteliai su įvairia skirtingos koncentracijos maistine soda, stiklainis gyvybės, ampermetras, voltmetras, elektrinis smiginis, raktas, elektrodas, termometras, elektrinė viryklė.
Pasirinkite instaliaciją pagal schemą;
Ant plytelės uždėkite 4% grub sodos;
Įjunkite plytelę;
Ištaisyti temperatūros skirtumą;
Patikrinkite ampermetro ir voltmetro rodmenis per odos laipsnių skirtumą;
Razrahuvat opіr, kad elektroprovіdnіst formules.
Kad būtų išlaikytas 4% charchovoy sodos produkcijos pūdymas, jie pradėjo šildyti temperatūrą papildomu termometru.
3 lentelė
Skirtumas procentais nuo I (A) U (B) R (Om) λ (cm)
4 18 1 6 6 0,17
19 1,03 6 5,83 0,172
20 1,05 6 5,71 0,175
21 1,08 6 5,56 0,180
22 1,1 6 5,45 0,183
λ=1R (1Ω=Sm)
Visnovok: Akivaizdu, kad elektros laidumas didėja kylant temperatūrai. Kaitinant, jonų greitis didėja, o krūvių perkėlimas iš vieno taško į kitą netrukus paspartės.
Grafikas 1. Temperatūros skirtumo atramos gylis.
2 grafikas. Elektros laidumo gylis priklausomai nuo temperatūros
Visnovok
Perskaitę literatūrą apie soda, її zastosuvannya galią medicinoje, žolelių pramonėje, užpakaliuką, atlikę daugybę pastebėjimų, padarėme išvadą, kad:
Soda - bagatolika kalbos, mokyklų mainai volodіє rіznimi institucijos
Opіr rozchinu sodos nuosėdos jogo koncentracijoje.
Nuo koncentracijos priklauso ir skirtumo elektrinis laidumas.
Elektros laidumas dėl temperatūros svyravimų didėja.
Literatūra
Žagalnos cheminiai tyrimai. Dėl raudonos. aš. P. Muchlionovas. Vis. chemijos-technologinių specialybių asistentas. - M: Viščios mokykla.
Pasaulinės chemijos pagrindai, 3 v., B. V. Nekrasovas. - M: Chemija, 1970 m.
Žagalnos cheminiai tyrimai. Furmer I. E., Zaicevo g. N. - M .: Vishcha mokykla, 1978 m.
Zagalna khіmіchna rozrobka, red. aš. Volfkovich, t. 1, Soda M. - L., 1953, p. 512-54;
Benkivsky g., Technologija sodoproduktiv, M, 1972;
Šokinas I. N., Krasheninnikov Soda A., Sodos technologija, M., 1975 m.
Kas žino vairuotojo mokyklos valandų formulę? Aišku, viskas. Manau, kad iš pačių chemijos kursų pas turtinguosius, kurie paskui nesimoko ir nesispecializuoja, dingsta tik žinios, ką reiškia formulė H 2 O. Žemės planetoje neįmanoma.
Vandens jako kalba
Vandens molekulė, kaip atrodo, susideda iš vieno rūgštaus ir dviejų vandens atomų. Formulė parašyta taip: H 2 O. Kalbai gali būti suteikiamos trys būsenos: kieta – iš pirmo žvilgsnio į ledą, panaši į dujas – iš pirmo žvilgsnio, o reta – kaip medžiaga be spalvos, skonio ir kvapo. Prieš kalbą – vienintelė kalba planetoje, nes ji gali būti vartojama visose trijose šalyse vienu metu natūraliu protu. Pvz.: Žemės poliuose yra ledas, vandenynuose – vanduo, o po mieguistais iškilimais – garai. Kam vanduo anomalus.
Daugiau vandens yra plačiausia kalba mūsų planetoje. Vaughn dengia Žemės planetos paviršių gali būti šešiasdešimt šimtų tūkstančių - vandenynai, daugybė upių su ežerais ir ledo lytys. Daugiau vandens druskos planetoje. Vaughn netinka gerti ir stipriai gyventi. Gėlas vanduo tampa mažiau nei dviem su puse šimtosios dalies vandens, atsižvelgiant į vandens kiekį planetoje.
Vanduo yra dar stipresnis už tą yakіsny rozchinnik. Zavdyaki tsomu khіmіchnі rektsії vіdі praeiti іz didinga swedіstyu. Jėgos kaina įliejama į žmogaus kūno apsikeitimą kalbomis. kad septyniasdešimt šimtų metų suaugusio žmogaus kūnas susideda iš vandens. Vaiko vokai vis dar aukšti. Senatvėje šis ekranas nukrenta nuo septyniasdešimties iki šešiasdešimties tūkstančių metų. Prieš kalbą lyderio ypatumas iš karto parodo, kad gyvenimo pagrindas yra iškovotas pats. Kokio vandens organizme daugiau – Timas sveikas, aktyvus ir jaunas. Štai kodėl visų kraštų gydytojai nekaltai tvirtina, kad reikia daug gerti. Žiūrėkite į patį švarų vandenį, o ne į arbatinukus, ieškodami arbatos, kaip į kitus gėrimus.
Vanduo formuoja planetos klimatą ir nėra dominuojantis. Šiltos srovės vandenyne įkaitina visą žemyną. Tse vіdbuvaєtsya už rahunok, kad vanduo blėsta net gausiai mieguistas karštis, o tada vіddaє yogo, jei pradėsite pasiekti. Taigi jis reguliuoja planetos temperatūrą. Per daug turtinga sakyti, kad Žemė jau seniai būtų atvėsusi ir pavirtusi akmeniu, nėra taip, kad žaliojoje planetoje būtų toks didelis vandens kiekis.

Dominuojanti lyderystė
Vanduo gali būti turtingesnis nei іkavih valdžia.
Pavyzdžiui, vanduo – visa kito karto kalba. Gimnazijos kurso metu kažkas dainingai prisimena tokį supratimą, kaip vandens ratą gamtoje. Pavyzdžiui: stiklinė vandens išgaruoja veikiant tiesioginiams mieguistiems pokyčiams, virsta vandens garais. Dali, ši porelė vėjo pagalbai, kad būtų kur nors nugabenta, įliptų į sutemus, o paskui nukristų į kalnus pamačius sniegą, krušą ar lietų. Dali, iš gіr potіchok zbіgaє vėl žemyn, dažnai garuose. Ir taip – pagal statymą – ciklas kartojasi milijonus kartų.
Be to, vairuotojas turi didelę šilumos talpą. Pats per vandens baseinus yra daugiau vandenynų, dar lengviau pasiekiamas pereinant iš šiltojo ar į šaltąjį sezoną. Visų pirma, skirtingu temperatūros kilimo laiku vanduo dar labiau įkaista. Zavdyaki tsomu, kadangi jis turėjo būti didesnis, vanduo vėl stabilizuoja temperatūrą visoje mūsų planetoje.
Jei yra gyvsidabrio, vandens paviršiaus įtempimo vertė gali būti didesnė. Neįmanoma neprisiminti, kad ant lygaus paviršiaus tarsi puiki gėlė išsilieja lašelis. Kuriame pasireiškia visas vandens lankstumas. Dar viena galia joje pasireiškia, kai temperatūra nukrenta iki kelių laipsnių. Kai tik vanduo pasiekia ženklą, tampa lengva. Todėl ledas visada plūduriuoja vandens paviršiuje ir gaudo jį slenkant, purtydamas upes ir ežerus. Zavdyaki tsyomu prie vandenų, kurie užšaldo uzimką, neužšaldykite žuvies.
Vanduo kaip elektros laidininkas
Bent jau svarbu žinoti apie tuos, kurie yra laidūs elektrai (tai tik keletas). Elektros laidumas – kalbos kūrimo tikslas yra pravesti elektros srovę per save. Vіdpovіdno, elektroprovіdnіst vod - tse mozhlivіst vod strum. Tsya zdatnistst būti deponuotas tarp druskų kiekio ir kitų namų šalia šalies. Pavyzdžiui, distiliuoto vandens elektrinis laidumas gali būti sumažintas iki minimumo, kai toks vanduo yra išvalytas įvairiais priedais, nes tai būtina geram elektros laidumui. Pagrindinis strumos laidininkas yra jūros vanduo, kuriame druskų koncentracija jau yra didelė. Priklausomai nuo vandens temperatūros, elektros laidumas turėtų būti didesnis. Kuo aukštesnė temperatūros vertė, tuo didesnis vandens elektrinis laidumas. Tsya dėsningumas ilgą laiką buvo atskleistas mokslininkų fizikų skaitmeniniams įrašams.

Vimiryuvannya elektrinis vandens laidumas
Šis terminas yra konduktometrija. Taip vadinamas vienas iš elektrocheminės analizės metodų, pagrįstų konstrukcijų elektriniu laidumu. Zastosovuyt tsey metodas, skirtas nustatyti druskų ir rūgščių koncentraciją diapazonuose ir kontroliuoti kai kurių pramoninių variantų sandėlį. Vanduo gali būti amfoterinis. Tokiu būdu, pasitelkus protą, gera parodyti kaip rūgštį, o bazinį autoritetą - atlikti rūgšties vaidmenį, o pagrindo vaidmenį.
Priedas, kuris vikoristovuyut už šią analizę, aš netgi galiu eiti pagal pavadinimą - konduktometras. Konduktometro pagalba išmatuojamas elektrolitų elektrinis laidumas, kurį galima gauti iš pardavėjo, kurio analizė atliekama. Galbūt, varto paaiškinkite vieną terminą – elektrolitas. Tse speakovina, jakas, kai skiriasi arba ištirpsta, skyla į jonus, kuriems atliekama elektros srovė. Jonas – visiškai elektra įkrauta dalis. Vlasne konduktometras, remdamasis pagrindiniais vandens elektros laidumo vienetais, nustato vandens elektrinį laidumą. Tobto reiškia tam tikro vandens laidumo laidumą, imamą kaip burbuliukų vienetą.
Dar prieš praėjusio amžiaus aštuntojo dešimtmečio pradžią, norėdami nustatyti elektriko laidumą, jie įveikė vimiro „mo“ vienybę, ląstelė buvo panaši į kitą dydį - Ohm, kuris yra pagrindinis parama. Elektros laidumas – visa vertė, suvyniota proporcingai atramai. Tuo pačiu metu ji laimės „Siemens“. Vertė pavadinta mokslininko fiziko iš Nimechchini Wernerio fon Siemenso garbei.
Siemens
Siemens (gali būti žymimas kaip Cm, taigi i S) - ta pati vertė, pasukta į Ohm, kuris yra elektros laidumo vienetas. Vienas Divas yra brangesnis, ar tai būtų konduktorius, ar kažkoks vairuotojas 1 Ohm. Siemens išreiškiamas pagal formulę:
- 1 cm \u003d 1: Ohm \u003d A: B \u003d kg −1 m −2 s³A², de
A - amperas,
V - voltas.

Vandens šilumos laidumas
Dabar pakalbėkime apie tai – kalbos pastatymas gali perduoti šiluminę energiją. Reiškinio esmė ta, kad atomų ir molekulių kinetinė energija, kuri lemia tam tikro kalbos kūno temperatūrą, її vzaєmodії perduodama kitam kalbos objektui. Priešingu atveju šilumos laidumas yra toks pat, kaip šilumos mainai tarp kūnų, plyšių ir navitas tarp kūnų ir plyšių.
Vandens šilumos laidumas taip pat didesnis. Žmonės šiandien laimi lyderio galią, patys to neminėdami. Pavyzdžiui, supilkite šaltą vandenį į indą ir atvėsinkite gėrime. Šaltas vanduo atima šilumą iš šokio, indo, natom_st duoda šaltį, galima ir nugaros reakcija.
Dabar tse reiškinys gali būti lengvai matomas planetos mastu. Vandenyną sušildo vasara, o tada – nuo šalto oro aš pilnai pasiekiu ir matau savo šilumą, šildančią žemynus pačius. Per žiemą atvėsęs vandenynas toje pačioje žemėje pradeda vis labiau atšilti ir suteikia vėsumą žemynams, kurie tvyro vasaros saulėje.

Vandens galia
Daugiau rozpovidalų apie tuos, kad žuvys gyvena prie vandens ir vėjai tos, kurios greitai gaudo vandenį visais paviršiais. Žinome, kad ledinis vanduo pradeda keistis esant nuliui laipsnių temperatūrai. Per tuos, kur vandens storis didesnis, mažesnis storis susilieja ir pagauna paviršių.
vandenų galia
Taip pat vanduo skirtingiems protams gali būti ir oksiduojantis, ir drėkinantis. Taigi vanduo, atiduodamas savo elektronus, yra teigiamai įkrautas ir oksiduojamas. Priešingu atveju elektronika užpildoma ir įkraunama neigiamai, ji taip pat įkraunama. Po pirmojo lašo vanduo oksiduojasi ir vadinamas mirusiu. Vaughn gali turėti dar daugiau baktericidinės galios, tik gėrimo ašis nereikalinga. Kitoje vapadoje vanduo gyvas. Iškovojo džiaugsmą, stimuliuojantį organizmą įkvėpimui, nešančią klitino energiją. Skirtumas tarp dviejų ir tos pačios galios parodomas terminu „oksidacijos-atkūrimo potencialas“.

Kodėl vanduo sukuriamas reguvati
Vanduo zdatna reaguoja mayzhe z usima upių, yakі є Žemėje. Vienintelis dalykas, kurio reikia norint patvirtinti šias reakcijas, yra užtikrinti tinkamą temperatūrą ir mikroklimatą.
Pavyzdžiui, kambario temperatūroje vanduo gerai reaguoja su tokiais metalais kaip natris, kalis, baris – jie vadinami aktyviaisiais. Su halogenais – ce fluoru, chloru. Kaitinamas vanduo gerai reaguoja su šalčiu, magniu, vandeniu, metanu.
Įvairių katalizatorių pagalba vanduo patenka į reakciją su amidais, karboksirūgščių esteriais. Katalizatorius - cerechovina, nibi pіdshtovhuє komponentai iki abipusės reakcijos, kuri bus greičiau.
Či yra deindės vanduo, Žemės krislas?
Kol kas Sonyach sistemos planetoje, Žemės Kryme, vandens nebuvo atskleista. Taigi jie pripažįsta, kad palydovuose yra tokių milžiniškų planetų kaip Jupiteris, Saturnas, Neptūnas ir Uranas, tačiau tikslių duomenų dar nėra. Egzistuoja dar viena hipotezė, kol likusi jos dalis nebuvo patikrinta, apie požeminius vandenis Marso planetoje ir Žemės palydove – Mėnulyje. Kai Marsas buvo pakeltas, mokslininkai numatė žemas teorijas apie tuos, kurie buvo šioje planetoje, buvo vandenynas, ir kad modelis gali būti navigacinis.

Sonyachny sistemos laikysena grindžiama beasmenėmis didžiosiomis ir mažosiomis planetomis, de, už vchenih įleidimo gali būti vandens. Ale, kol kas niekaip negaliu dainingai persirengti kitu.
Kaip praktiniais tikslais pakeisti vandens šilumos laidumą elektros energijai
Kreipdamasis į tuos, kad vanduo turi didelę šiluminę galią, jis vibruoja prie šilumos tinklų kaip šilumos nešiklis. Tai užtikrins šilumos perdavimą iš spozhivačiovo pašaro. Yra daug atominių elektrinių, kaip šilumą nešantis vanduo.
Medicinoje vicor naudojamas aušinimui, o pora - dezinfekcijai. Taigi pats švino vikoristovuyut viešojo maitinimo sistemoje.
Turtinguose branduoliniuose reaktoriuose akvariuminis vanduo naudojamas kaip sėkmingo Lanzug branduolinės reakcijos veiksnys.
Vanduo, esantis po pergalės yda, yra kaltas skaldymui, pralaužimui ir vyniojimui kalnų veislių pjovimui. Tse aktyviai vikoristovuєtsya už tunelių, požeminių įrenginių, sandėlių, metro gyvenimą.
Visnovok
Zі statti vyplivaє, scho vandens už savo autoritetą ir funkcijas - svarbiausia ir priešiška kalba Žemėje. Či atiduoti žmogaus gyvybę, nesvarbu, ar tai būtų kitas gyvas gyvenimas Žemėje vandenyje? Tikrai taip. Chi spryaє tsya kalba apie žmonių mokslinės veiklos žinias? Taigi. Ką gali padaryti vanduo? Vidpovidas irgi „taip“. Insha upė, sho švinas Žemėje, o tada daugiau švaraus vandens, mažiau daedalų. І mūsų užduotis yra išsaugoti ir apsaugoti її (ir taip pat, і mus visus) įvykio metu.
Kuo skiriasi elektrinis ir TEN katilas?
Prie TEN katilo papildomai elektrai šildomas TEN - vamzdinis elektrinis šildytuvas, kuris vėliau tiekia šilumą šilumnešiui. Elektrinis katilas veikia srauto pravedimui per šilumnešį (vanduo arba šilumnešis, kuris neužšąla, "-20 C"). Vibruojančios strumos praėjimas negali būti vadinamas elektrolize; Elektrinis katilas yra paprastas ir net perkaitintas vandens šildytuvas (radianas) idealiomis sąlygomis, jį galima dirbti nekeičiant daugybės uolienų (dešimčių akmenų) elementų.
Kuo elektrinių katilų aptarnavimo terminas prideda praktiškumo?
Elektrodinio katilo veikimui būtina, kad katilo darbui (pitomy laidumu) būtų reikalinga šilumą nešanti maka. Elektrodinis katilas yra opalinės sistemos dalis. Kad katilas veiktų patikimai ir be problemų, deginimo sistema privalo atitikti rekomenduojamus katilo pase parametrus.
Kodėl šildymo sistemos su elektriniais katilais skamba ekonomiškai ir kokybiškai?
Nepriklausomai nuo sulenkimo, kai paleidžiamos degimo sistemos, pagrįstos elektriniais katilais, elektriniai katilai yra ekonomiški TEN atžvilgiu, mažiausiai 20–30%. Elektrinių katilų ekonomiškumą nusveria daugiau nei 15 metų trunkanti montavimo ir eksploatavimo praktika. Patikimumą ir ekonomiškumą užtikrina paprastesnis, geresnis dizainas. Prie DEŠIMT katilo ŠĖŠĖLIAI įkaista, o tada ŠEŠĖLĖS suteikia šilumos namams. Elektrodų katile pati tėvynė atlieka šildymo vaidmenį. Kai struma praeina, tėvynė įkaista visu tūriu, kuris yra katile. Vykoristovuyuchi elektrodny radiatorių šildymas, esant panašiam įtempimui, galima keisti katilo tūrį kilka kartų.
Esant tinkamai parinktai sistemai, katilas paleidžiamas esant mažam (mažiau nei 50%) vardiniam slėgiui, o įšilęs palaipsniui didina slėgį. Šiuolaikinė automatika leidžia reguliuoti komfortišką temperatūrą patalpoje +/- 0,2 laipsnių tikslumu. C. Esant išdegintam zam_sky budinki, galima įveikti tyzhny režimą deginimui naudojant deginimo sistemą. Tokiu būdu robotų elektrinių katilų ekonomiškumas pasiekiamas:
- mažesnė inercija kaitinant (šprotams);
- sklandi pradžia;
- zastosuvannya moderni automatika;
Patikimumą ir ilgaamžiškumą užtikrina dizaino paprastumas ir modernių medžiagų kaupimas.
Kiek elektros galite sutaupyti katilui?
Katilas valgė patogiau. energijos, kurios sumuoja gyvenimo šilumos suvartojimą.
Esant normalioms eksploatavimo sąlygoms, esant normaliam šilumos įvadui, tinkamai parinkus katilą, esant maksimaliam žiemos režimui (jei Kijevo gatvėse -23, kai įprastai sulankstoma degimo sistema, katilas kasybai veikia apie 8 metus (režimu įjungtas šildymas, įjungtas - vėsinimas ) Paimkime katilo slėgį, padaugintą iš 8 metų vidutiniškai ir paimkime elektros energijos mažinimą kasybai.
Kaip teisingai pasirinkti katilą?
Elektrinis katilas "ION" parenkamas pagal šiuos parametrus:
- 1 kW intensyvumo elektrodinis katilas gali apšildyti patalpas iki 20 kv/m, iki 60 kubinių metrų ir 40 litrų vandens deginimo sistemoje.
Pavyzdžiui, - 5 kW šiluminės galios katilas gali šildyti patalpą, kurios plotas yra 100 kv / m, kurio tūris yra 300 kubinių metrų, o vandens kiekis degimo sistemoje - iki 240 litrų. .
Kaip su ION elektriniu katilu galima apdeginti vamzdžius ir radiatorius?
Kai kurios sistemos gali būti pergalės, nesvarbu, ar tai trimitai, kaip ir šio sertifikato atveju. Rekomenduojame naudoti polipropileną.
Vikoristannya metaloplastikovyh vamzdžiai nebazhano, spoluchn_ jungiamosios detalės suttvo zvuzhuyut artimųjų pereriz;
metalinis-plastikinis vamzdis dažnai yra silpnas iki deformacijos ir išsiplėtimo esant kolivavimo temperatūrai.
Galima vikruoti ar tai modernūs radiatoriai (chavun, bimetal), ar geresni vicoristate plieniniai akumuliatoriai. Chavunnі radiatoriai vikoristovuvat unbazhano, į tai, kad smarvė gali turėti didelį tūrį tėvynėje, porėtos struktūros, kad atkeršyti brud viduryje.
Siekiant užtikrinti katilo ilgaamžiškumą ir patikimumą, dėl mažesnio paties katilo įleidimo ir išleidimo antgalio vidinio skersmens negalima kaltinti įvado ir išleidimo vamzdžių bei vamzdžių jungiamųjų detalių.
Kokie yra ION elektrinių katilų privalumai?
Katilų "ION" darbo kamera pagaminta iš specialios vamzdinės medžiagos, kuri jonizaciniams katilams yra dar svarbiau patikimumo ir ilgaamžiškumo požiūriu.
Praktiškai visų panašių katilų darbo kamera pagaminta iš plonasienės natūralaus vamzdžio medžiagos. Електроди котлів «ION» більшого діаметру виконані зі спеціального сплаву, що збільшує їхню довговічність та надійність при іонообмінному процесі, а також дає можливість формувати тепловий потік усередині камери котла з більшою швидкістю на відміну від котлів тих самих котлів інших виробників.
Katilai „ION“ pristatomi įvairiausių modelių, skirtų kitų markių katilams, kurie leidžia praplėsti gėrimo kiekį.
ION katilo katilas nesieja pirkimo prie savo šilumos perdavimo, o ION elektrinius katilus galima eksploatuoti, tų pačių katilų priežiūrai, su puikiu vandeniu arba savarankišku šildymo sistemos paruošimu degimo sistemoje.
Ar galite naudoti antifrizą šilumos perdavimo kokybei?
Būtina suprasti, kad antifrizas nėra skirtas naudoti deginimo sistemose. Vynas yra šlykštus! Geriau vikoristovuvat specialius neužšąlančius ridinius. Tačiau kadangi šių gamyklų aludariai neapsaugo savo elektrinio laidumo, tuomet juos perpumpavus į deginamąją sistemą galima atlikti visus tuos pačius paruošiamuosius darbus – sureguliuoti elektrinį katilą į reikiamą srovę (pranešama, kad procedūra aprašyta vadove operacijai). Iš praktikos galiu pasakyti, kad esant neužšąlančių kietų srautų ant elektrinio katilo fazės, yra tam tikrų priklausomybių - ir reikia praskiesti distiliuotu vandeniu (maždaug iki -5-10 gr užšalimo temperatūros. ).
І nepaprastai svarbu nepamiršti apie antifrizo galią:
- Antifrizo fizines galias iš esmės valdo fizinės vandens galios. Antifrizų šiluminė talpa 15-20% mažesnė, prie vandens mažesnė, klampumas 2-3 kartus mažesnis, tūrio plėtimasis 40-60% didesnis. Taip pat skiriasi šilumos laidumo, virimo temperatūros ir kitų fizinių savybių vertės. Tse reiškia, kad šildymo sistemoje naudojant antifrizą, reikia 40-50% padidinti radiatorių šilumos išmetimą, 40-50% padidinti išsiplėtimo bako tūrį, 60% padidinti cirkuliacinio siurblio slėgį. , pakeiskite daugybę kitų šildymo parametrų, be to, katilo skaičių ir slėgį.
- Kaip antifrizo temperatūra sistemoje, ji turėtų būti vienas iš trijų taškų (ir dažniausiai jis yra katilo kaitinimo elemento viduryje), viršijantis šiam antifrizo prekės ženklui kritinę vertę - etileno šiluminį plėtimąsi. glikolis ir kietosios antikorozinės rūgštys tirpaluose. Nukreipkite šilumos srautą per sistemą. Rūgštys sukelia metalų koroziją degimo sistemoje. Taip pat perkaitus antifrizui kyla putos, dėl kurių sistema atšaldoma, o esant šaltam orui – sustorėja kelmas ir susidaro kietos putos panašios nuosėdos. Pridėti priedų turėtų būti atliekama tol, kol antifrizas pradės cheminę reakciją su stiprintuvų medžiagomis - guma, paronita plonai, dėl ko dienos vietose atsirado nuotėkis. Be to, nepriimtina naudoti vamzdynus, kurių vidus yra padengtas cinko danga.
- Antifrizai gali padidinti įsiskverbimo galią arba jautrumą. Kuo daugiau sriegiuotų z'ednan, tarpiklių, susiaurėjimo, tuo lengviau atrodo ritė. Iš esmės posūkis dažnai kaltinamas dėl apdegimo, jei sistema šalta. Dėl aušinimo pasikeičia metaliniai vamzdžiai ir dėl to atsiranda mikrokanalų, tokių kaip antifrizas. Todėl visos deginimo sistemos išdegimo priežastys turi būti prieinamos apžiūrai ir taisymui, o tai reiškia, kad degančios sistemos įrengimas yra nepriimtinas. Antifrizai etilenglikolio pagrindu yra toksiški (vienkartinė mirtina dozė 100-300 ml), todėl jų negalima naudoti vandens šildymui GWP sistemose, o jei šilumokaičiai nesandari, karšto vandens išleidimo angose gali sunaudoti smarvės šukes. . Antifrizas taip pat yra toksiškas ir nėra kaltas dėl to, kad prasiskverbia iš gyvenamųjų patalpų.
- Yakshcho tu turi nemažą viborą I Virishi Vikoristovati neužšąlančio rydino karščio anchistry, Zupiniti Vibir kalaviją neužšąlusiems puodams "upelis 40", Ale Sliz į Setriye. nuo paronito!
Ar galima ION elektrodo katilą naudoti kartu su cirkuliaciniu siurbliu?
Elektrodinis katilas - šildymo srauto tipas, o tinkamam robotiniam katilui ir deginimo sistemai su cirkuliaciniu siurbliu būtina užtikrinti šilumos srautą per katilą su tokiomis indikacijomis:

Ar montuojant elektrodinį katilą reikia montuoti bet kokio skersmens vamzdžius?
Apdegimo sistemoje rekomenduojama dirbti prie elektrinio katilo įleidimo ir išleidimo angų, kurių vamzdžiai yra ne mažesni kaip 1 colio skersmens, deginimo sistemoje. Po šukavimo plovimui galite pereiti prie mažesnio skersmens vamzdžių, todėl bendras mažesnio skersmens vamzdžių pjūvis nebus mažesnis nei 1 colis.
Kaip šildyti namus, kurių plotas didesnis nei 750 kV/m?
Koks darbas, pavyzdžiui, mano taikymo sritis yra 2800 kV / m?
2800 kV / m plotui reikia įrengti mini katilinę, kurią sudaro 4 elektriniai katilai "ION" 3/36, po vieną lygiagrečiai. Vienoje vandens deginimo sistemoje lygiagrečiai (to paties slėgio) pajungus du ar daugiau elektrinių katilų „ION“, degimo zonos plotas (tūris) padidėja 2 ir daugiau kartų.
Pavyzdžiui: dvi modifikacijos 3/36 sudegina 1500 kv/m plotą, 4500 kubinių metrų tūrio, trys modifikacijos 3/36 išdegina 2250 kV/m plotą, 6750 kubinių metrų tūrio. ir kt.
Ar galima eksploatuoti elektrinį katilą be cirkuliacinio siurblio?
Jonizacijos kamera, demonstruojanti kaitinimo procesą, nedidelį išsiplėtimą, kitą staigų šilumos perdavimo padidėjimą ir dėl to jogos spaustuko skatinimą (su maksimaliu tvirtinimo įtempimu - iki 2 atmosferų). Taigi, ION elektrinis katilas gali būti naudojamas deginimo sistemose be cirkuliacinio siurblio, nes deginimo sistema pasirenkama natūralios cirkuliacijos schemai.
Ar galima jungti lygiagrečiai su kitais katilais?
Elektrinis katilas gali būti montuojamas lygiagrečiai su kitais katilais (dujiniais, kietos ugnies ir kt.) ir gali būti naudojamas Jums patogiu metu.

Norint paleisti elektrodo katilą, reikalingas ampermetras.
Prijungus katilą prie deginimo sistemos, srovės galia sumažinama ampermetru. Tuo atveju, jei srauto galia yra didesnė nei nurodyta katilo pase, į deginimo sistemą būtina įpilti distiliuoto vandens. Jei strumos stiprumas yra mažesnis nei būtina, į deginimo sistemą reikia įpilti kaustinės (charchov) sodos su rozmarinu 30 gramų 100 litrų vandens, sumaišant sodą šiltame vandenyje.
Ar galima naudoti elektrinį katilą "ION" degančiose sistemose su aliuminio radiatoriais?
Taigi, galima, saugoti tik sodos skirtumą elektros laidumui gerinti, reikia vijoti ASO-1 (speciali konstrukcija aliuminio radiatoriams)
Kaip yra šalies vikoristovuetsya sistemoje deginimo už valandą darbo elektrodų katilo "ION"?
Elektrodinio katilo "ION" darbo valanda nereikalauja specialaus šilumos perdavimo skysčių paruošimo. Yogo robotas pergalingas vanduo su augintinio elektrine atrama yra ne didesnis kaip 1300 omų div. Išsklaidytas vanduo yra elektrinio žibinto elementas, kuris mato šilumą, tam reikės pasiruošti dainuoti, norint paimti reikiamą elektrinį opirą (pvz., pabandyti pašildyti distiliuotą vandenį, nepavyks, nepavyks reikia leisti elektros srovę). Pasiruošti paskutiniam būdui – pakeisti vandens elektrinį atramą, įpilant šarminės (harchovos) sodos, arba skatinti distiliuotu (mediniu, taliniu) vandeniu. Viskas esą aprašyta elektrinių katilų pase.
Ar galite naudoti ION elektrinį boilerį karšto vandens tiekimui?
Elektriniai katilai "ION" gali būti naudojami kartu su netiesioginiais šildymo katilais karštam vandeniui tiekti, pavyzdžiui, elektrinis boileris "ION" 3/9 gali būti naudojamas iki 180 m2 ploto, iki 3 metrų aukščio. o vandens tūris sistemoje 360 litrų, prijungiant netiesioginį šildymo katilą, reikia iš karto pridėti šilumos slėgį karšto vandens tiekimui (HWP) pagal jūsų katilo paso duomenis, pavyzdžiui, 3/6 kW norint apdeginti kabiną ir HWP, jums reikia katilo, kurio šilumos slėgis yra 3/9 kW + 3/ 6 kW = 3 / 15 kW
Ar galima vienu metu naudoti elektrinį elektrodinį katilą "ION" iš "šilumos tiekimo" sistemos?
Vandens šilumos tiekimas - vamzdžių sistema uždaryta, roztashovannyh prie trauklių ir prijungta prie deginimo sistemos. Garso vikoristovuyutsya metaloplastikovy vamzdis per montavimo paprastumą. Šiluma po rąstu gali būti sumušta kaip pagrindinis arba papildomas deginimas. Iki valandos miego, šiltas vanduo su elektriniu boileriu „ION“ gali pasiekti didesnį ekonominį efektą.
Vandens tiekimo šiluma gali būti žema. Zavdyaki didelis paviršiaus augimas yra šilumos kiekis, kuris yra gyvybingas, aplaidžiai perduodamas svarbiausiems objektams. Tokiu būdu šilumos tiekimas užtikrinamas tolygiai horizontaliai ir vertikaliai paskirstant šilumą visoje naudojimo srityje.
Ar galite suprantamai paaiškinti, kaip paruošti šilumos nešiklį?
Jei naudojate opiatų sistemą kaip šilumą nešantį natūralų vandenį, tuomet būtina užtikrinti vandens atsparumą GOST R 51232 „Pitna vanduo“ (1300 omų kubiniam cm).
Negalite augti Vitsogo namų mintyse be specialaus turto. Bet gerti galima ir kitaip.
Pradedant eksploatuoti ION elektrinį katilą, būtina ampermetru išmatuoti pradinį strypą, naudojant strypo laidų spaustukus (arba tiesioginio įjungimo ampermetru).
Taigi, paleidžiant, strypo galia neatitinka paso numeriui priskirtų parametrų, atlikite šiuos veiksmus:
- Mažesnis strumas – būtina dalimis dėti sodos rozchino (keičiant pitomy opir rіdini). Pirmasis etapas yra ne daugiau kaip arbatinis šaukštelis šimtui litrų vandens (šilumos perdavimas). Vos po 2 metų stūmoklis padidėjo, pirmasis žingsnis kartojosi nežymiai.
- Smulkinkite daugiau – įpilkite distiliuoto arba sumedėjusio (taloї) vandens (bus daugiau geriamojo opir radini).
Ar galite pasakyti, kiek dar reikia nusipirkti medžiagų ir ar reikia dirbti, kad katilą paleistumėte į robotą?
Aiškus papildomų medžiagų ir įrangos, skirtos vienfazės jonų deginimo sistemos įrengimui ir paleidimui, sąrašas.
Obovjazkovas :
- Magnetinis starteris (kontaktorius) atitinka šio ION modelio strypo charakteristikas.
- Automatiškai vimikach (automatinis) vienpolis, mokyklų mainai v_dpov_daє strumovym charakteristikos šio modelio "ION".
- Elektros kabelis (elektros laidas) virš pjūvio atitinka šio modelio "ION" strypo charakteristikas. Elektros kabelis (elektros laidas), skirtas termostatui prijungti (pavyzdžiui, 3x0,5 (0,75) arba pv 3x0,5 (0,75).)
- ASO -1 (aliuminio radiatorių soda pakeitimas), nes sistemoje sumontuoti aliuminio radiatoriai, siekiant pagerinti vandens elektrinį laidumą
- Boksas (dėžė) paleidimo įrangos montavimui.
- Tiesioginio prijungimo ampermetras (vimiryuvalni klіshі), skirtas valdyti darbinę įtampą ir, jei reikia, laiku koreguoti šilumos laidumą.
- Kontrolinė lemputė rodo katilinę (šildymas, pertrauka, elektros tiekimas/prieinamumas rūsyje).
- Naujausias programuotojas SALUS FL091 skirtas papildomai taupyti energiją ir patogesnę deginimo sistemą
Zahisne įžeminimas OBOV'YAZKOVO!
Degimo sistema:
Norint palengvinti ION katilo darbą ir žymiai sutaupyti elektros energijos, būtina naudoti cirkuliacinį siurblį. Apdegimo sistema yra apsaugota papildomais vožtuvais, skirtais katilo ir siurblio rankiniam aptarnavimui, montavimui ir išmontavimui.
O kas yra gražiau už trifazę Kazanę?
Palikite viską, priklausomai nuo to, kokią įtampą turite - 220 arba 380.
Kaip jūs turite galimybę sumontuoti katilą ant trijų fazių 380 V. , Vіd 3/6 kW, tse suteikia papildomos naudos. Trifaziuose katiluose sumontuotos trys elektros, kurias galima dažnai įjungti, pvz., ION katile 3/6 kW yra trys 2 kW elektriniai, ne sezono metu, jei lauke +10 laipsnių šilumos reikia įjungti katilą visu intensyvumu, ir pakanka įjungti vieną elektrodą. Jei neturite trijų fazių, galite įrengti trifazį katilą vienai fazei. Fazė yra padalinta į tris išėjimus ir ateina per automatinius įrenginius iki trijų elektrodų. Trifaziai katilai dotsilino vikoristati vіd 100 kv.m.
Kokios problemos gali kilti montuojant tarpinius vamzdžius?
Renkantis deginimo sistemą iš vidutinių vamzdynų, svarbi problema yra midi su kitais metalais įvedimas vienoje vandens cirkuliacijos sistemoje. Beperedny z'єdnannya midi plieno, cinkuoto plieno ar aliuminio atveju sukeliama elektrocheminė reakcija, dėl kurios skiriasi salė, cinkas ir aliuminis. Ir taip pat neįmanoma įveikti vamzdžio kaip įžeminimo elektrotechnikos elemento. Norint išjungti šį reiškinį, būtina turėti vandenį izoliuojantį pamušalą. Navit dėl metalinės lazdelės, kuri skatina protingesnių medžiagų koroziją. Šis procesas yra midi jonų, kurie matomi apgulties metu (Cu2 +), prasiskverbimo į vandenį rezultatas tolygios vidutinių paviršių korozijos procese. Jie yra nusiminę korozinių skydelių vietose, kurios jau yra viniuotos, šaukdamos greičiau sugriauti pagrindinės medžiagos (plieno, cinkuoto plieno ar aliuminio). Prie labiausiai nesaugių korozijos formų guli virazkova ir erozinis.
Virazkovy korozija, є vietinė metalo korozija, atsiranda ruinuvannya oksido lydymo vietose, kurios dengia vidinį vamzdžių, kurie liečiasi su vandeniu, paviršių. Prie šalto ir karšto vandens tiekimo vamzdžių nuleiskite faktorių ir palengvinkite šalto vandens sutvarkymą, arba ausys jau naudojamos pagrindiniam vandeniui:
- neteisingas chemijos sandėlio midi,
- neteisingas vamzdžių vidinių paviršių paruošimas jų gamybos procese,
- Aš lituosiu laidą ant vidinio vamzdžių paviršiaus,
- kietųjų dalelių buvimas vamzdžių viduryje (pavyzdžiui, pisku), kurios įsiskverbė į įrenginį montavimo metu arba per pirmąją veikimo valandą (filtravimo garsas gali būti tiekiamas į sistemą, todėl її promyvannya) .
Erozinę koroziją sukelia turbulentinis vandens išsiliejimas ant vamzdžių sienelių. Esant tokiam rangui, svarbu užbaigti projektinį vandens srauto srautą, taip pat išjungti mechanines atramas, pavyzdžiui, zondavimą, įpylimą į lydmetalį, neteisingą vandens bakstelėjimą.
Apdegimo sistemose plieno ir midi sumažinimas yra priimtinesnis, jei rūgštumo kiekis vandenyje neviršija 0,1 mg/dm3, o uždarose sistemose tai praktiškai įmanoma mažiau. Varinių ir aliuminio radiatorių nerekomenduojama montuoti uždaroje cirkuliacinėje sistemoje.
Ar galima deginimui naudoti elektrinį katilą, kaip aš turiu šildymo kištuko (PZV) įrenginių elektros instaliacijose?
Praktinė srovės ritės vertė nustatoma pagal izoliatorių konstrukciją ir yra ties 20 ¬ 40 mA riba. Tuo pačiu metu ypatingas dėmesys turėtų būti skiriamas, kai šildymas prijungiamas prie elektros linijos iš papildomo jungiklio (PZV), kad galėtumėte užregistruoti strumos ritę 30 ¬ 40 mA diapazone.
Žvelgiant į kainą, tokio tipo šildymą reikia jungti per automatinį jungiklį, apeinant ELV.
Kaip galiu gauti galiojantį sertifikatą jūsų gaminiams?
Mūsų įmonė švenčia penkiolika metų nuo elektrinių (joninių) katilų kūrimo ir parinkimo. Pirmą kartą Ukrainos rinkoje pristatome energiją taupantį naujos kartos elektrinį deginamąjį priedą "ION".
Pasiruošimas naudoti naujas technologijas ir šiuolaikines medžiagas. Patobulintas dizainas ir atnaujintas elektrodo lydinys su trivalio terminu vikoristannya.
Elektrinis apdegimas "ION" atliekamas pagal technines nuostatas ir projektinę dokumentaciją.
Iš kokybės sertifikato galite sužinoti paspaudę paveikslėlį.


Vanduo yra unikali kalba, nes ji gali susilankstyti savo molekulinę struktūrą, nes dar nėra susukta iki galo. Nepriklausomai nuo agregatinės būsenos, H2O molekulės yra susipynusios viena su kita, o tai reiškia beasmenes lyderio ir її razchinіv fizines galias. Supraskime, kodėl vanduo yra laidus šilumai.
Apie pagrindines fizines H2O galias galima pamatyti:
- sustorėjimas;
- skaidrumas;
- spalva;
- kvapas;
- mėgavimasis;
- temperatūra;
- drovumas;
- radioaktyvumas;
- šilumos ir elektros laidumas.
Likusios vandens šilumos laidumo ir elektrinio laidumo charakteristikos jau yra nestabilios ir slypi gausiuose faktoriuose. Pažvelkime į jų ataskaitą.
Elektrinis laidumas
Elektros srovė yra vienpusis neigiamo krūvio dalelių – elektronų judėjimas. Deyakі speakovina gali perduoti qi dalis, o deyakі - nі. Tsya zdatnіst vyyavlyaєtsya skaitine forma ir є elektros laidumo vertė.
Verta aptarti, koks gali būti švaraus vandens elektrinis laidumas. Laimėjo zdatna diriguoti šturmą, bet tai dar blogiau. Distiliato elektrinis laidumas paaiškinamas tuo, kad H2O molekulės dažnai skyla į H+ ir OH- jonus. Elektrodalelės perduodamos padėti teigiamai įkrauti jonus vandenyje, pastatai juda vandenyje.
Kodėl reikia nustatyti upės elektros laidumą
H2O elektrinis laidumas nusėda dėl tokių veiksnių kaip:
- joninių namų buvimas ir koncentracija (mineralizacija);
- jonų prigimtis;
- temperatūros
- vandens klampumas.
Pirmieji du veiksniai yra pradiniai. Todėl, apskaičiavę gimtosios žemės elektros laidumo reikšmes, galime spręsti apie mineralizacijos lygį.
Gamta neturi gryno vandens. Navit zherelna є kakiy rozchin druskos, metalai ir kiti elektros namai. Ce sampruoti jonai Na+, K+, Ca2+, Cl-, SO4 2-, HCO3-. Taip pat į sandėlį gali patekti silpna elektra, dėl kurios galios atlikti štangą labai nepakinta. Prieš juos matyti Fe3+, Fe2+, Mn2+, Al3+, NO3-, HPO4 – ir kt. Didesnės koncentracijos metu gali būti mažesnis smarvės elektrinio laidumo įtekėjimas, kaip, pavyzdžiui, nuotekų vandenyse iš virobnitstv išleidimo angų. Tsikavo, kad esantys namai prie vandens, tarsi išgyventų ledo stotyje, neįteka į pastatą vesti elektros.
Jūros vandens elektrinis laidumas
Jūros vandenį geriau leisti elektrine srove, nuleiskite gėlą vandenį. Tai paaiškinama nayavnistyu in nіy razchinenoї druska NaCl, kaip geras elektrolitas. Padidėjusio laidumo mechanizmą galima apibūdinti taip:
- Natrio chloridas, atskirtas nuo vandens, skyla į Na + ir Cl- jonus, kurie gali sukelti skirtingus krūvius.
- Jie yra Na +, traukiantys elektronus, kad galėtų sukelti esamą krūvį.
- Rukh natrio jonai tovshch sukelia elektronų poslinkį, o tai savo rankomis sukelia elektros srovės sunaikinimą.
Tokiu būdu vandens elektrinis laidumas yra akivaizdus tų kitų namų druskose. Mažiau čiurlenkite, daugiau žemesnių pastatų praleidžia elektros srovę. Su distiliuotu vandeniu Won praktiškai lygus nuliui.
Vimiryuvannya elektros laidumas
Vimiryuvannya elektroprovidnosti razchinіv zdіysnyuєtsya už papildomus konduktometrus. Tse spetsialnі priladi, dii yakikh ґruntuєtsya principas dėl spіvvіdnoshennia elektroprovіdnostі ir namų koncentracijos-elektrolitivinės analizės. Šią dieną yra beasmenių modelių, pavyzdžiui, pastato vimiryuvat elektros laidumą ne tik didelės koncentracijos veislių, bet ir gryno vandens, kuris yra distiliuotas.
Šilumos laidumas
Šilumos laidumas - fizinės kalbos konstrukcija praleidžia šilumą iš įkaitusių dalių į šaltas. Vanduo, kaip ir kitos kalbos, turi tokią galią. Šilumos perdavimas vyksta iš molekulės į H2O molekulę, kuri yra molekulinis šilumos laidumo tipas, arba judančiam vandens srautui - turbulentinis tipas.
Prie šprotų vandens šilumos laidumas kitoks, kitose retose upėse mažesnis, už išsilydžiusių metalų – jie turi visą ekraną.
Pastato vanduo praleidžia šilumos nuosėdas dėl dviejų veiksnių: slėgio ir temperatūros. Didėjant slėgiui, laidumo rodiklis didėja, temperatūra pakyla iki 150 ° C, padidėja, tada pradeda mažėti.
Kodėl vanduo baseinuose mums šaltas
Vandens šilumos laidumas kilkoje dešimtis kartų viršija tą pačią vertę kiekvieną kartą. Jei žmogus yra peršlapęs prie vandens ar tiesiog juo apipiltas, padidėja šilumos nuostoliai, todėl esant tokiai temperatūrai jis tampa šaltesnis, žemesnis. Tai matyti iš programų, nukreiptų į lentelę:
Sužinokite faktus apie vandenį: vaizdo įrašas
Oksidacijos stadija +1.
Su puse natrio senosiomis valandomis. Natrio chloridas yra būtinas žmogaus gyvenimo komponentas.
C skaitoma, kad žmonės pradėjo gyventi neolite, tobto. arti 5–7 kukmedžių. to likimas.Pagal Senąjį įsakymą tai skamba kaip kalba „neter“. Tsya kalba buvo pergalinga kaip miyuchy zasib. Geriau už viską, neter - soda, natrio karbonatas, kuris įsitvirtino sūriuose Egipto ežeruose ir iš garų krantų. Graikų autoriai Aristotelis ir Dioskoridas bei senovės Romos istorikas Plinijus Vyresnysis rašė apie šią kalbą, nors ir pavadinimu „nitron“, jogą vadindami jau „nitrum“.
XVIII amžiuje chemikai jau žinojo apie gausų natrio kiekį. Natrio druskos buvo plačiai naudojamos medicinoje, verčiant odas, kimšant audinius.
Natrio metalą pašalino ankstesnis anglų chemikas ir fizikas Humphrey'us Devi, elektrolizuodamas išlydytą natrio hidroksidą (su 250 porų vario ir cinko plokštelių). Vardas "
natrio “, Mergelės malda už šį elementą Na2CO 3 . Lotyniškas ir rusiškas fermentacijos elemento pavadinimas iš arabiško žodžio „natrun“ (natūrali soda).Natrio išplėtimas gamtoje ir jogos meistriškumas. Natris – somis iš plačiausių elementų ir penki iš plačiausių metalų (po aliuminio, cinko, kalcio ir magnio). Jogas vietoj žemės plutos tapti 2,27%. Daugiau natrio perkama iš įvairių aliumosilikatų sandėlio.Natrio druskų didybė prilygsta grynai išvaizdai visuose žemynuose. Smarvė yra senovės jūrų išgaravimo rezultatas. Šis procesas, kaip ir anksčiau, yra trys Druskos ežere (Juta), Negyvojoje jūroje ir kitose vietose. Natris jungiasi ir atrodo kaip chloridas
NaCl (galit, kam'yana sil), taip pat karbonatas Na 2 CO 3 NaHCO 3 2 H 2 O (tronas), NaNO nitratas 3 (nitratas), sulfatas Na2SO410H2O (Mirabilitas), tetraboratas Na 2 B 4 O 7 10 H 2 O (boraksas) ir Na 2 B 4 O 7 4 H 2 O (Kernitas) ir kitos druskos.Nevicherpnі natrio chlorido atsargos є natūraliuose rozoluose ir vandenyno vandenyse (apie 30 kg m -3). Skaičiuojama, kad akmens stiprumas, prilygstantis natrio chloridui Šviesiajame vandenyne, užimtų 19 milijonų kubinių metrų. km (50 proc. daugiau, Šiaurės Amerikos žemyno apatinė danga yra aukščiau nei jūra). Tokio obsyagu prizmė іz ploscheyu substav 1 kv. km gali pasiekti Mіsyatsya 47 kartus.
Bendras natrio chlorido kiekis iš jūros vandens siekė 6–7 mln. tonų vienoje upėje, tai yra beveik trečdalis visų lengvųjų rūšių.
Gyvoje kalboje vidurkis yra 0,02% natrio; būtybės turi daugiau jogo, žemesnės – roslinų.
Paprastos kalbos ypatybės ir metalo natrio formuluotė. Natris – sidabriškai baltas metalas, plonais rutuliukais su purpuriniu atspalviu, plastiškas, minkštas (lengvai pjaustomas peiliu), gaiva natrio kibirkštis. Natrio elektros laidumo ir šilumos laidumo vertės yra didelės, storis yra 0,96842 g / cm 3 (esant 19,7 ° C), lydymosi temperatūra yra 97,86 ° C, virimo temperatūra yra 883,15 ° C.Potrito lydinys, kuriame yra 12 % natrio, 47 % kalio ir 41 % cezio, turi žemiausią metalo sistemų lydymosi temperatūrą – -78°С.
Natrio ir jogos zabarvlyuyut pusiau šviesiai ryškiai geltonos spalvos. Poline natrio spektro linija patvirtina perėjimą 3
s 1–3 p 1 elemento atomai.Didelis natrio cheminis aktyvumas. Vynų paviršiuje skystis pasidengia peroksido, hidroksido ir karbonato mišiniu. Rūgštyje dega fluoras ir natrio chloridas. Kai spalyuvanni metalo peroksidas nusėda ant paviršiaus.
Na2O 2 (su namo oksidu Na2O ).Esant aštriai natrio reakcijai, jau trinant prie stebulės, į aštrų tašką įpilama sieros rūgšties arba įpilama sulfido. Kietasis anglies dioksidas („sausasis ledas“) vibruoja, kai liečiasi su natriu (anglies dioksido gesintuvai, skirti gesinti natrio, kuris dega, negali stovėti!). Naudojant azotą, elektros išlydžio reakcija yra dar mažesnė. Nesąveikauti natrio su inertinėmis dujomis.
Natris aktyviai reaguoja su vandeniu:
Na + 2 H 2 O = 2 NaOH + H 2Reakcijos metu matomos šilumos pakanka metalui ištirpti. Tam, tarsi šalia vandens išmestas mažas natrio gabalėlis, dėl reakcijos šiluminio poveikio jis ištirpsta ir vandens paviršiuje „didelis“ už vandens guli metalo lašas. varomas matomo vandens reaktyviosios jėgos. Su natrio alkoholiais sąveikauja sodriai ramiai, mažiau su vandeniu:
Na + 2 C 2 H 5 OH \u003d 2 C 2 H 5 ONa + H 2Natris yra lengvai atskiriamas retu amoniaku su ryškiai juodais metastabiliais variantais dėl neįsivaizduojamų galių. Esant -33,8 ° C, 1000 g amoniako ištirpina iki 246 g metalo natrio. Razvedeni rozchini išlieta mėlyna spalva, koncentruota - bronzos spalvos. Smarvė gali likti šalia jūsų. Nustatyta, kad reto amoniako natrio vidurys yra jonizuotas:
Na Na + + e Reakcijos lygybės konstanta yra dorіvnyu 9,9 10 -3. elektronas, kur jis patenka, yra ištirpinamas amoniako molekulių ir sudaro kompleksą [
e(NH3) n ] - . Otrimanі rozchini mayut metalo elektroprovіdnіst. Išgarinant amoniaką, išsiskiriantis metalas prarandamas. Esant nereikšmingam vynų dispersijos išsaugojimui, žingsnis po žingsnio metalo reakcija su amoniaku su patvirtintu amidu NaNH 2 arba imidu Na 2 NH Mačiau vandenį.Jie taupo natrią po vandens žievės kamuoliu (dujos, mineralinė alyva), mažiau veža iš lituotų metalinių laivų.
Elektrolitinis pramoninio natrio ekstrahavimo metodas sugedus 1890 m. Elektra buvo tiekiama tirpstant natrio hidroksidui, kaip ir Mergelės atveju, bet su pergalėmis buvo tobulesnė energija, mažesni voltai. Šiame procese, atsižvelgiant į natrio, matoma rūgšta:
katodas (zalizny):
Na + + e - = Naanodas (nikelis): 4
OH - - 4 e - \u003d O 2 + 2 H 2 O .Gryno natrio chlorido elektrolizės metu kaltinamos rimtos problemos, kurias pirmiausia sukelia artima natrio chlorido lydymosi temperatūra ir natrio virimo temperatūra, o kitu būdu – didelė natrio įvairovė retame natrio chloride. Pridėjus natrio chlorido, kalio chlorido, natrio fluorido, kalcio chlorido, lydymosi temperatūrą galima sumažinti iki 600°C.
NaCl ir 60% CaCl 2 ~580° W viduryje, sukurtą amerikiečių inžinieriaus G.Downso, 1921 metais sukūrė Dupont šalia elektrinės netoli Niagaros krioklių.Ant elektrodų vyksta šie procesai:
katodas (zalizny):
Na + + e - \u003d Na Ca 2+ + 2 e - \u003d Caanodas (grafitas): 2
Cl - - 2 e - \u003d Cl 2 .Metalinis natris ir kalcis nusėda ant cilindrinio plieno katodo ir pakyla už papildomo vamzdelio, kuris atvėsta savotišku kalcio kietumu ir vėl patenka į lydalą. Chloras, kuris nusėda ant centrinio grafito anodo, surenkamas po nikelio plokšte ir išvalomas.
Narazі obsyag vyrobnitstvva metalo natіyu įdėti kіlka tysyach tonų už rіk.
Metalo natrio pergalės pažadą su joga sieja stiprios įkvepiančios jėgos. Ilgą laiką didžioji dalis vibruoto metalo nugalėjo dėl tetraetilo švino
PbEt 4 ir tetrametilšvinas PbMe 4 (benzino antidetonatoriai) alkilchlorido reakcija su natrio lydiniu ir švinu esant aukštam slėgiui. Ninіtse virobnitstvo greitai veržiasi per zabrudnennya dovkіllya.Kita zastosuvanijos sritis – titano, cirkonio ir kitų metalų bei jų chloridų gamyba. Turėjimui naudojamas mažiausiai natrio vikario, pavyzdžiui, hidrido, peroksido ir alkoholio.
Natrio, kaip vertingo katalizatoriaus, dispersija gumos ir elastomerų gamyboje.
Augantis išlydyto natrio, kaip šilumokaičio, kaupimasis branduoliniuose reaktoriuose ant skystų neutronų. Žema natrio lydymosi temperatūra, mažas klampumas, mažas neutronų perkaitimas turi nepaprastai aukštą šilumos laidumą ir šilumos laidumą, todėl jogas (ir jogo lydinys su kaliu) yra nepakeičiama medžiaga šiems tikslams.
Natrієm nadіyno išvalo transformatorių olії, eterius ir kitą organinę kalbą vandens pėdsakų pavidalu, o dėl papildomų natrio amalgamų galite lengvai pavadinti vandenį sodriais sluoksniais.
Pusė natrio. Natris patenkina naują suvartojimo rinkinį su svarbiausiais anijonais. Svarbu, kad tokiais atvejais būtų praktiška pridėti krūvį tarp katijoninės ir anijoninės kristalinių uolienų dalių.natrio oksidas
Na2O sintezuoti reakciją Na 2 O 2, NaOH , bet trumpiau apie viską NaNO 2, su metaliniu natriu:Na 2 O 2 + 2 Na \u003d 2Na 2 O2NaOH + 2Na \u003d 2Na2O + H2
2 NaNO 2 + 6 Na = 4 Na 2 O + N 2Likusioje reakcijos dalyje natris gali būti pakeistas natrio azidu
NaN 3: NaN 3 + NaNO 2 = 3 Na 2 O + 8 N 2Sutaupykite natrio oksido geriau nei bevandenį benziną. Vynas yra įvairių sintezių reagentas.
natrio peroksidas
Na2O 2 blyškiai geltonuose milteliuose, jis ištirpsta, kai oksiduojamas su natriu. Su tuo, turint mintyse sausas tiekimas sausas rūgštus (pakartokite) oksidas nusėda ant burbuolės. Na2O , kuris vėliau virsta peroksidu Na2O 2. Dėl rūgštingumo natrio peroksidas yra termiškai stabilus iki ~675° C .Natrio peroksidas plačiai naudojamas pramonėje kaip pluošto, popieriaus masės, vilnos ir kt. tepalas. Vіn є stiprus oksidatorius: vibruoja sumishi su aliuminio milteliais arba kaimuose kalvose, reaguoja su sirkoy (kai pasidaro karsta), uzima turtinga organine zeme. Natrio peroksidas, sąveikaudamas su anglies monoksidu, ištirpina karbonatą. Natrio peroksidui reaguojant su anglies dioksidu, pastebimas rūgštingumas:
Na 2 O 2 + 2 CO 2 \u003d 2 Na 2 CO 3 + O 2Ši reakcija gali būti svarbesnė už praktinį zastosuvannya laukinių aparatų povandeniniams darbuotojams ir ugniagesiams.
natrio superoksidas
NaO 2 otrimuyut su visišku natrio peroksido kaitinimu 200-450 ° temperatūroje, esant 10-15 MPa slėgiui. Įrodyk nušvitimą NaO 2 anksčiau buvo pašalintos iš rūgščio reakcijos su natriu, disperguotos retame amoniake.Supilkite vandenį į natrio superoksidą, kol šaltyje pasirodys rūgštus:
NaO 2 + H 2 O \u003d NaOH + NaHO 2 + O 2Kylant temperatūrai didėja matomo rūgštumo kiekis, tai kaip išsidėsto iki natrio hidroperoksido:
NaO 2 + 2 H 2 O \u003d 4 NaOH + 3 O 2Natrio superoksidas yra uždarų patalpų regeneravimo sistemų komponentas.
Natrio ozonidas
Na O 3 ištirpsta, kai praskiedžiamas iki ozono bevandenio natrio hidroksido milteliuose žemoje temperatūroje, naudojant įžeidžiančią chervono ekstrakciją Na Apie 3 retas amoniakas.natrio hidroksidas
NaOH dažnai vadinamas kaustine soda arba natrio hidroksidu. Tse yra tvirtas pagrindas, joga atnešama į tipiškas pievas. Skaitmeniniai hidratai buvo paimti iš natrio hidroksido pasiskirstymo vandenyje. NaOH nH 2 O de n = 1, 2, 2,5, 3,5, 4, 5,25 ir 7.Natrio hidroksidas yra agresyvesnis. Vіn ruynuє slo і porcelianas, skirtas rahunok vzaєmodії z silicio dioksidas, scho mіstsya juose:
NaOH + SiO 2 \u003d Na 2 SiO 3 + H 2 OPavadinimas "skysta soda" atspindi natrio hidroksidą, kuris atsirado ant gyvų audinių. Ypač nesaugus yra vyčio kalbos smūgis.
Orleano hercogo Nicolas Leblanc Likaras (
Leblanas Nikolajus ) (1742-1806) 1787 m. sukūrė rankinį natrio hidroksido ekstrahavimo iš NaCl (1791 m. patentas). Šis pirmasis didelio masto pramoninis cheminis procesas tapo didžiuliu technologiniu laimėjimu Europoje XIX amžiuje. P_znіshe procesas Leblanc buv vіsneniya elektrolitichnym protsess. 1874 metais p. šviesos vibracija į natrio hidroksidą sudarė 525 tūkst. t, s 495 kukmedis. t buli otrimani už Leblanc metodą; iki 1902 metų natrio šarmo koncentracija siekė 1800 tūkst. t., protezas Leblanc metodu buvo nuimtas mažiau nei 150 kukmedžių. t.Šiandien natrio hidroksidas yra svarbiausia pieva pramonėje. Didžioji dalis produkcijos yra mažesnė nei 10 mln. tonų JAV. Elektrolizuojant natrio chloridas ištirpsta natrio hidroksidas ir susidaro chloras:
katodas (zalizny) 2
H 2 O + 2 e - \u003d H 2 + 2 OH anodas (grafitas) 2
Cl - - 2 e - = Cl 2Elektrolizė lydi pievos koncentraciją didžiuosiuose viparyuvachuose. Didžiausias pasaulyje (gamykloje
PPG Industries Lake Charles ) gali būti 41 m aukščio ir 12 m skersmens. b -naftolis, natrio druskos (hipochloritas, fosfatas, sulfidas, aliuminatas) Be to, natrio hidroksidas zastosovuetsya gaminant popierių ir plaušienos, medaus ir miyuchih zasobiv, aliejus, tekstilės gaminius. Vynas būtinas boksitų perdirbimui. Svarbi natrio hidroksido taikymo sritis yra rūgščių neutralizavimas.natrio chloridas
NaCl įvadas virtuvės druskos, akmens druskos pavadinimais. Vіn pagaminti bebarežių mažai higroskopinių kubinių kristalų. Natrio chloridas lydosi 801 ° C temperatūroje, verda 1413 ° C temperatūroje. NaCl , o esant 80 ° C - 38,12 p.Natrio chloridas yra būtinas prieskonis, kuris yra nepakeičiamas. Anksčiau stiprumas buvo lygus aukso kainai. Senovės Romoje legionieriams dažnai buvo mokamas ne centas, o kupiūra, kuri skambėjo kaip kareivio žodis.
Netoli Kijevo Rusios gimė slenksčiai iš Karpatų regiono, iš druskingų ežerų ir Juodosios bei Azovo jūrų estuarijų. Vaughn brangiai kainavo lovas, kurios buvo patiektos ant garbingų svečių stalų urochistų šventei, o kiti buvo išbarstyti „ne sūria duona“.
Astrachanės sričiai atėjus į Maskvos valstybę, Kaspijos jūros ežerai tapo svarbiais druskos marškinėliais ir vis tiek її neišlipo, buvo kelias, dėl to kaltas pačių įvairiausių gyventojų nepasitenkinimas. , kaip išaugo per maištą, Druskos riaušės (1648 m.) vardu.
1711 m. Petras I pamatė dekretą dėl druskos monopolio įvedimo. Žemės pardavimas tapo valstybės viniatkovy teise. Druskos monopolis atsirado antroje rokivo pusėje ir buvo skasovana 1862 m. roci.
Devyni natrio chloridas yra rastas produktas. Kartu su akmenimis vugills, vapnyak ir sirkoy vin patekti į vadinamąjį "Didžiojo ketverto" mineralinį syrovina, geriausią chemijos pramonės šaltinį.
Daugiausia natrio chlorido yra Europoje (39 proc.), Šiaurės Amerikoje (34 proc.) ir Azijoje (20 proc.), o Šiaurės Amerikoje ir Okeanijoje – mažiau nei 3 proc., o tik Afrikoje – 1 proc. Kam'yana priverčia didžiąsias požemines gentis (dažnai šimtus metrų vėjo malūno), todėl atkeršyti daugiau nei 90 proc.
NaCl . Tipiška Češyro druskų šeima (Didžiojoje Britanijoje natrio chloridas Dzherelo) apima 60ґ 24 km, o atstumas iki druskos sluoksnio yra arti 400 m.Svitovy obsyag vidobotku druska ant burbuolės 21 valg. siekia 200 mln. tonų, 60% chemijos pramonės (chloro ir natrio hidroksido, taip pat popieriaus masės, tekstilės, metalų, dervos ir alyvuogių gamybai), 30% - Charchova, 10% tenka kitoms veiklos sritims. Pavyzdžiui, natrio chloridas naudojamas kaip pigi priemonė nuo apledėjimo.
natrio karbonatas
Na2CO 3 dažnai vadinama soda arba tiesiog soda. Vynmedžiai auga gamtoje matant sumaltas rožes, sūrymus ežeruose ir mineralus Na 2 CO 3 10 H 2 O, terminis natris Na 2 CO 3 H 2 O, palieskite Na 2 CO 3 NaHCO 3 2 H 2 O . Natrio raminamoji medžiaga, pvz. Na 2 CO 3 7 H 2 O, Na 2 CO 3 3 NaHCO 3, aKCO 3 nH 2 O, K 2 CO 3 NaHCO 3 2 H 2 O .Iš pramonės turimų balų elementų druskų svarbiausias yra natrio karbonatas. Dažniausias jogos pergalės būdas yra belgų chemiko technologo Ernsto Solvay 1863 metais sukurtas metodas.
Natrio chlorido ir amoniako vandeninio tirpalo koncentracijos nedideliu slėgiu užpildomos anglies dioksidu. Kuriame taške nusodinamas homogeniškai žemos kokybės natrio bikarbonatas (kintamumas
NaHCO 3 tampa 9,6 g 100 g vandens 20 ° C temperatūroje):NaCl + NH 3 + H 2 O + CO 2 = NaHCO 3Ї + NH 4 Cl Norėdami pašalinti soda, natrio bikarbonatas kepamas: NaHCO 3 \u003d Na 2 CO 3 + CO 2 + H 2 OMatoma, kad anglies dioksidas virsta pirmojo proceso metu. Dodatkovu kіlkіst kіlkіst іkіdіkі uglezyu vyyut rahunka rahuvannya zharyuvannya kalcio karbonatas (vapnyaku):
CaCO 3 \u003d CaO + CO 2Kitas reakcijos produktas - kalcio oksidas (vapno) - amoniako regeneravimo su amonio chloridu vieta:
CaO + 2 NH 4 Cl \u003d CaCl 2 + 2 NH 3 + H 2 OTaigi, vienintelis šalutinis sodos gamybos Solvay metodu produktas yra kalcio chloridas.
Visiškai lygus procesui:
NaCl + CaCO 3 \u003d Na 2 CO 3 + CaCl 2Akivaizdu, kad aukščiausių protų sąmonėje vandenyje vyksta atvirkštinė reakcija, pavydo šukės šioje sistemoje perkeliamos dešiniarankiai į dešinę dėl nesuderinamumo su kalcio karbonatu.
Soda, pašalinta iš natūralaus sirovino (natūralios kalcinuotos sodos), gali sumažinti sodos kokybę, pašalinta amoniako metodu (chlorido pašalinimas yra mažesnis nei 0,2%). Be to, kapitalo investicijos ir sodos suderinamumas su natūralia sirovina yra 40–45% mažesnis, mažesnis nei sintetinio būdo. Beveik trečdalis lengvųjų sodos produktų iš karto patenka į natūralias gentis.
Svіtove virobnitstvo
Na2CO 3 1999 pakilo su įžeidžiančiu laipsniu:| Usyogo | |
| Pivn. Amerika | |
| Azija/Okeanija | |
| Zachas. Europa | |
| cx. Europa | |
| Afrika | |
| Plat. Amerika |
Jungtinėse Amerikos Valstijose didžioji dalis pasaulio šalių praktiškai labiau slypi sintetinės sodos pelenų pavidalu. Kita vieta pasaulyje, kurioje po JAV gaminama kalcinuota soda, yra Kinija. Šios cheminės medžiagos gamyba Kinijoje 1999 m. siekė apie 7,2 mln. tonų.
Turtingais atvejais natrio karbonatas pakeičiamas natrio hidroksidu (pavyzdžiui, pašalinus popieriaus masę, saldus, naudingas valymui). Beveik pusė natrio karbonato yra pramonės stiklo pakaitalai. Viena iš plėtojamų spūsčių sričių – nuosėdų šalinimas iš energetikos pramonės dujų telkinių ir geležies krosnių. Į natrio karbonatą, kuris reaguoja su sieros dioksidu ir ištirpusiais kietais produktais, natrio sulfatą, įpilkite miltelių, kad būtų galima filtruoti arba nusodinti.
Anksčiau natrio karbonatas buvo plačiai naudojamas kaip „pralna soda“, tačiau dabar kaitinimo sfera atsirado per Viktoriją kituose stebuklinguose agentuose.
natrio bikarbonatas
NaHCO 3 (charchovos soda), zastosovuetsya, pirmaujanti vieta, kaip anglies dioksido ugnis verdant duoną, ruošiant konditerijos gaminius, dujinius gėrimus ir gabalėlį mineralinio vandens, kaip gaisro gesinimo sandėlių ir likarsky zasib sudedamoji dalis. Tse pov'yazano z patogus sulankstymas esant 50–100° Z.natrio sulfatas
Na2SO 4 Zustrichaetsya gamtoje bevandenės išvaizdos (tenarditas) ir dekahidrato (mirabilitas, Glauberio stiprumas). Vіn įeikite į sandėlį astrahonіtu Na 2 Mg (SO 4) 2 4 H 2 O, vantofitas Na 2 Mg (SO 4) 2, glauberitas Na 2 Ca (SO 4) 2 . Didžiausios natrio sulfato atsargos yra prie NVS sienų, taip pat JAV, Čilėje ir Ispanijoje. Mirabilitas, natūralių druskingų ežerų aboa sluoksnių vizijos, išdaigos 100 ° C temperatūroje. Vikorovtvoy produkto vikoristano sirchany rūgšties aukos sulfatas, o produktas yra vibracijos kiekis, jaki, Yaki, į kelią, į kelią, į kelią, į keliąDuomenys apie natrio sulfato rūšis neskelbtini, tačiau, remiantis skaičiavimais, natūralaus sirovino šviesos gamyba yra beveik 4 milijonai tonų vienoje upėje. Apskaičiuota, kad natrio sulfato, kaip šalutinio produkto, emisija yra 1,5–2,0 mln. tonų.
Ilgą laiką natrio sulfatas yra šiek tiek vikoristas. Dabar kalba yra popieriaus pramonės pagrindas, šukės
Na2SO 4 є kaip pagrindinis reagentas sulfatinės celiuliozės preparate, skirtame rudos spalvos popieriui ir gofruotam kartonui ruošti. Medienos drožlės arba tirsas paverčiami karštu balos natrio sulfatu. Gaminame ligniną (medienos komponentą, kuris suriša pluoštus) ir celiuliozės pluoštus, kuriuos ištiesiname popieriaus gamybos mašinoje. Rozchin, scho zalishivsya, virkite, kol vynai pažadins pastatą, degindami, suteikdami augalui garą ir šilumą virimui. Sulfato ir natrio hidroksido lydymasis yra stabilus, kol išnyksta, ir gali būti perdirbtas.Mažiausia natrio sulfato dalis sustingsta, kai susidaro toksiški patogenai. Hidratuota forma
Na2SO410H2O (Glauberio jėga) є nešiojama rankomis. Ninі iškovojo pergales mažiau, o anksčiau nusileido.natrio nitratas
NaNO 3 vadinamas natriu arba Čilės nitratu. Didelės natrio nitrato nuosėdos, aptiktos Čilėje, akivaizdžiai nusėdo biocheminio organinių pertekliaus paskirstymo pagalba. Amia, kuri buvo pastebėta vietoje, buvo humovirno, oksiduota iki azoto ir azoto rūgščių, o po to reagavo su įvairiu natrio chloridu.Pašalinkite natrio nitratą molio azoto dujoms (bendrai azoto oksidai) karbonatu arba natrio hidroksidu arba kalcio nitratą pakeitę natrio sulfatu.
Natrio nitratas zastosovuyut kaip gerai. Vynas yra retų druskų šaldymo agentų, marinavimo vonių metalo apdirbimo pramonėje, šilumos kaupimo sandėlių sudedamoji dalis. Pinigų kaina nuo 40 proc.
NaNO 2, 7 % NaNO 3 ir 53 % KNO 3 gali virėti lydymosi temperatūroje (142° C) iki ~600° C. Natrio nitrato vikoristas kaip oksidatorius vibuchovinėse kalbose, raketų gaisruose, pirotechnikos sandėliuose. Vіn zastosovuєtsya natrio druskų, įskaitant nitritą, pavidalu, kuris tarnauja kaip maisto produktų konservantas.Natrio nitritas
NaNO 2 gali būti pašalintas iš terminio natrio nitrato plėtimosi arba jogos: NaNO 3 + Pb = NaNO 2 + PbOKomercinei natrio nitrito gamybai sugerkite azoto oksidą vandeniniu natrio karbonatu.
Natrio nitritas
NaNO 2 krіm vikoristannya su nitratais šilumai laidžių lydalo kokybės, plačiai zastosovuєtsya gaminant azobarvnikiv, korozijai slopinti ir mėsos konservavimui.Olena
Savinkina LITERATŪRA Populiarios cheminių elementų bibliotekos. M., Nauka, 1977 mGreenwood N.N., Earnshaw A. Elementų chemija, Oksfordas: Butterworthas, 1997 m